氯化钠溶解度
Release Time:2020-12-30氯化钠溶解度介绍
本文中介绍了氯化钠,溴化钠和溴化钾在溶剂水中的溶解度,甲醇,乙醇和甲醇+乙醇,以及溴化钠在水中的混合物+甲醇和在水+乙醇混合溶剂中测定溴化钠和氯化钾的范围使用分析重量法在298.15和348.15 K之间 如果可能,可靠性通过将实验数据与文献数据进行比较来检验该方法。 方法证明与所报告的数据相比,其溶解度通常可重现在文学中。
氯化钠,溴化钠和溴化钾在溶剂水中的溶解度介绍:
含盐体系中相平衡的研究对于许多工业应用来说非常重要。更多特别是,需要准确的溶解度知识用于分离工艺的设计,例如萃取结晶1或为了安全操作不同的处理单元(例如蒸馏塔,吸收单元,2它们也可用于将溶解度与离子半径或其他可能相关的理论研究溶剂化参数3和用于计算盐的溶解度乘积或离子对缔合常数Pitzer-Simonson4或Clegg-Pitzer5方程。而对于水性电解质系统,溶解度为通常可用于许多盐,即在Stephen和Stephen6,7或Linke和Seidell,8,9的汇编书中用于有机溶剂或水性有机混合溶剂数据非常稀缺,过时或根本不可用2。因此,一个用于系统测量的程序是用于测量NaCl,NaBr,KCl,和KBr的温度范围介于298.15和353.15 K在纯溶剂中的水,甲醇和乙醇及其二元混合溶剂溶剂组成范围。由于已经通过实验测量了一些溶解度,10,11在这项工作中,最后的一系列测量被呈现。
氯化钠溶解度实验部分:
化学品:在所有实验中,蒸馏去离子水被使用了。所有其他化学品均由XXX公司提供;盐纯度高于99.5%的NaCl,KCl和NaBr最低纯度为的溶剂甲醇和乙醇使用99.8%,无需进一步纯化。避免水盐污染,盐在393.15 K干燥炉使用2天以上。程序。该程序的详细说明有因此,仅给出了用于进行测量的分析重量分析方法的简要说明11。该方法包括准备一个恒温((0.1 K)。平衡池充满已知质量((0.1 mg)所有成分,并达到溶液平衡在此条件下,在搅拌条件下至少搅拌3小时。工作温度。然后让溶液沉降在用加热的注射器采样之前至少需要1/2小时。的总溶剂蒸发分两个阶段完成。原来,将样品放在加热板上,以增强形成盐晶体,然后将其完全干燥在393.15 K的烤箱中。样品保留在烤箱中超过3天,然后在干燥机中用硅胶1天。最后,将它们称重,然后定期重复此过程,直到质量恒定实现。每个实验点的平均值至少为遵循以下之一的三种不同测量标准。如果溶解度高于10(质量百分比),那么{2s} / {solubility}×100的商应小于小于0.1,其中s是一组内的标准偏差
不同的实验结果。如果实验溶解度小于10%,则很难达到此标准,而标准偏差s应该小于0.005。
氯化钠溶解度实验结果与讨论
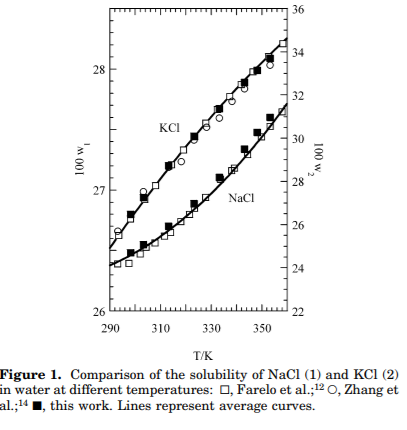
二进制系统。 在表1中,测得的溶解度不同水,甲醇和乙醇中盐的含量报告温度。 水+盐系统是在298.15至353.15的温度范围内进行了研究K,而对于含甲醇的系统,最大值温度为333.15K。仅在三种不同温度下进行了研究:298.15,323.15和348.15 K,因为盐的溶解度也太大低或温度依赖性不明显。可以对测量数据的质量进行调查通过将其与汇编书籍6-9和公开文献; 为了水+盐二元系统,比较起来很容易之所以这样做,是因为发布的数据量很大。在某些情况下,汇编书足以使平均曲线适合与最近的图形进行更好的图形比较。对于系统,如图1所示。水+氯化钠和水+氯化钾。 从图1可以看出可能会观察到数据的良好一致性,即使系统地衡量了这项工作中的溶解度更高时(每100克溶液约含0.05克氯化钠)与Farelo等人的值比较12。
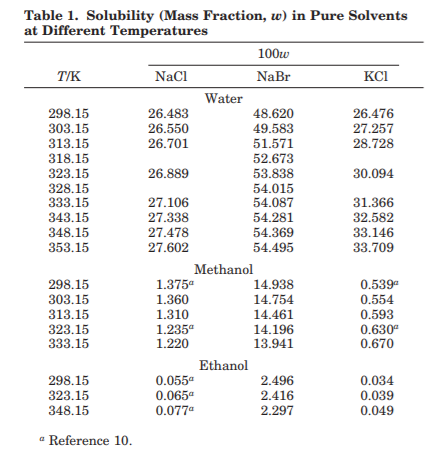
图1
Farelo和合作者报告的数据显然在更好地符合平均曲线,他们使用了多热合成法,不是最足够,因为温度几乎没有影响NaCl的溶解度13。他们显示出意外的不规则趋势的原因低温下的实验数据,因为直到300 K时溶解度几乎都是恒定的。比较此处测得的溶解度和溶解度Farelo等人12报道了水+ KCl不同的温度,有可能在图中观察。
见下期说明.......



 购物车
购物车 



