酶抑制剂(Enzyme inhibitors)类产品介绍(竞争性抑制剂,非竞争性抑制剂,)
Release Time:2019-11-05酶类制剂介绍
酶抑制剂介绍:酶抑制剂作用是与酶结合并降低其活性的分子, 由于阻断酶的活性可以杀死病原体或纠正代谢失衡,因此许多药物都是酶抑制剂,酶抑制剂同时还应用于杀虫剂中。 当然并非所有与酶结合的分子都是抑制剂,酶激活剂与酶结合并增加其酶促活性,而酶底物则在酶的正常催化循环中结合并转化为产物。
抑制剂主要可分为:竞争性和非竞争性抑制剂
1.竞争性抑制剂
这是最直接,最明显的酶抑制形式,通过该名称可以准确告诉您发生了什么。
该抑制剂具有与酶的通常底物相似的形状,并且与它竞争活性位点。但是,一旦将其连接到活动站点,就不会发生任何事情。它没有反应-本质上,它只是阻碍。
酶与底物反应的一般方程:

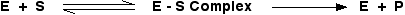
竞争性抑制剂的等效方程:

复合物不会进一步反应形成产物,但其形成仍然是可逆的,它再次分解形成酶和抑制剂分子。
如果您增加底物的浓度,则底物可以与抑制剂竞争,因此正常反应可以合理的速率发生。
一个简单的例子涉及丙二酸根离子抑制琥珀酸脱氢酶。该酶催化琥珀酸根离子向富马酸根离子的转化。现代名称是:
- 丙二酸酯:丙二酸酯
- 琥珀酸酯:丁二酸酯
- 富马酸酯:反丁烯二酸酯
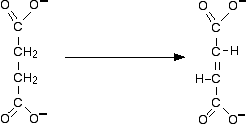
该反应被丙二酸根离子所抑制,丙二酸根离子的形状与琥珀酸根离子非常相似。
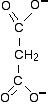
相似的形状使丙二酸根离子结合到活性位点,但是离子中心缺少CH2-CH2键会阻止进一步的反应发生。
因此,丙二酸离子会阻止活性位点-但请记住,这是可逆的。丙二酸离子将分解并再次释放酶。丙二酸根离子正在争夺该地点-它们并未破坏它。
如果琥珀酸根离子的浓度高于丙二酸根离子,那么它们比丙二酸根离子更容易进入该部位。这意味着您可以通过增加底物的浓度来克服竞争性抑制剂的作用。
注意:有些生物化学家对使用化学名称非常草率!如果您在其他地方读到此反应,则可能会发现该反应被引用为将琥珀酸转化为富马酸。有些消息甚至暗示“琥珀酸”和“琥珀酸”是同一意思。从化学角度来看,这是不可接受的!
据发现,正确的版本是从琥珀酸根离子到富马酸根离子的转化(如上所述)。在典型的细胞pH值约为7的情况下,这些物质将主要以其离子形式存在,而不是以联合酸形式存在。研究这种转化机理的人们的科学论文都谈论离子,而不是酸。
2.非竞争性抑制剂
非竞争性抑制剂不会自身附着于活性位点,而是附着于酶的其他位置。通过附着在其他地方,它会影响酶的结构,从而影响酶的工作方式。因为抑制剂和底物之间没有任何竞争,所以增加底物浓度无济于事。
如果您在网络上浏览各种生物化学网站,则会发现两种解释。我们将在一分钟内详细介绍一下简单而又显而易见的细节。我想先简短介绍一下另一个。
- “纯”非竞争性抑制剂
我发现了几个生化站点,这些站点说像这样工作的抑制剂(他们描述为纯非竞争性抑制剂)实际上是未知的。作为非生物化学家,我不知道这是什么真相-如果您想找出答案,您可能必须要获得生物化学学位!
- 其他非竞争性抑制剂
一些非竞争性抑制剂不可逆地附着在酶上,因此使酶永久停止工作,其他人则可逆地依附。在相当熟悉的情况下,一个非竞争性抑制剂的相对简单的例子是:
重金属中毒:您可能已经知道,包含重金属(例如铅,汞,铜或银)的化合物是有毒的。这是因为这些金属的离子是几种酶的非竞争性抑制剂。




 购物车
购物车 



