苯磺酸(制备、性质、用途)
Release Time:2022-01-241. 苯磺酸的制备:
苯磺酸由苯磺化制得。 为此,苯与浓硫酸一起加热。
C6H6 + H2SO4(concentrated) → C6H5SO3H + H2O
2. 苯磺酸实验室方法:
要在实验室中制备苯磺酸,在圆底烧瓶中取一份苯和两份浓硫酸的混合物。 将回流冷凝器连接到烧瓶上。 将烧瓶放在热水器上,在 80 -100°C 下加热约两小时。
此后,将混合物冷却并放入水中。 它含有碳酸钡。 未使用的硫酸沉淀为硫酸钡。 过滤它并分离它。 苯磺酸铍盐因溶于水而被过滤。
过滤后冷却,得到苯磺酸铍盐晶体,分离这些晶体,加入适量硫酸。 硫酸铍沉淀并释放苯磺酸。
过滤和分离硫酸铍沉淀物。 滤液冷却后得到含有苯磺酸结晶的水。 经分离加热得到无水苯磺酸(C6H5SO3H.3/2H2O)酸。
3. 苯磺酸物理性质:
苯磺酸是一种无色结晶固体。 它的熔点是65°C。 其含水晶体的熔点为 47°C。 它更易溶于水。

4. 苯磺酸化学性质:
其化学反应可分为三个部分。
-SO3H 基团的 -OH 基团参与的反应。
–SO3H 基团被取代的反应。
原子核的置换反应。
5. 苯磺酸 -SO3H 基团的 -OH 基团参与的反应:
酸性症状:它是一种酸。 其水溶液呈强酸性。 其水溶液的酸强度与硫酸一样高。 它与碱反应形成盐。
例:C6H5SO3H + NaOH → C6H5SO3Na + H2O
与五氯化磷反应:苯磺酸与五氯化磷反应时,-SO3H基团的-OH基团被氯原子取代。
C6H5SO3H + PCl5 → C6H5SO2Cl + POCl3 + HCl
与醇反应:与其他酸一样,它与醇反应形成酯。
C6H5SO3H + C2H5OH → C6H5 – SO2 –O – C2H5 + H2O
6. 苯磺酸 –SO3H 基团被取代的反应:
氢原子置换:苯磺酸用过热蒸汽或稀HCl或稀H2SO4加热分解,发生水分解得到苯。
C6H5SO3H + H2O → C6H6 + H2SO4
羟基置换:苯酚是通过将其钠盐或钾盐与固体 NaOH 或 KOH 熔化而获得的。
C6H5SO3Na + NaOH → C6H5OH + Na2SO3
胺基置换:苯胺是通过将其钠盐或钾盐与 NaNH2 或 KNH2 熔融而获得的。
C6H5SO3Na + NaNH2 → C6H5NH2 + Na2SO3
氰基置换:氰基苯是通过将其钠盐或钾盐与 NaCN 熔融而获得的。
C6H5SO3Na + NaCN → C6H5CN + Na2SO3
羧基置换:其钠盐或钾盐与亚磷酸钠熔炼,制得苯甲酸。
C6H5SO3Na + HCOONa → C6H5COOH + Na2SO3
-SN 基团置换:通过将其钠盐或钾盐与 KSH 熔融获得苯硫酚。
C6H5SO3K + KSH → C6H5SH + K2SO3
7、苯磺酸原子核的置换反应
磺酸基团是间位导向基团。 因此,从其卤化、硝化和磺化获得间位产物。 像所有其他元导演组一样,它也是一个停用组。 这意味着它的取代反应发生的强度低于苯。 以下是其主要的核取代反应。
卤化:在卤素载体存在下与氯复制时,形成间氯苯磺酸。
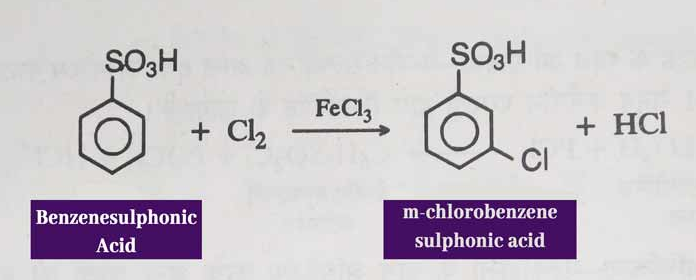
8. 苯磺酸硝化作用:当与浓NHO3和浓H2SO4的混合物加热时,会形成间硝基苯磺酸。
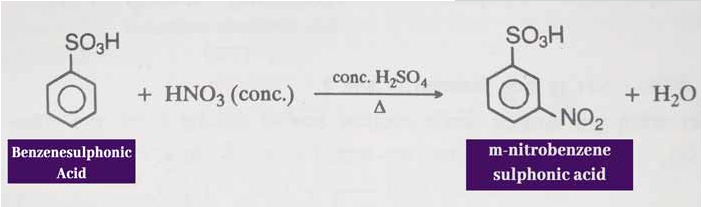
9. 苯磺酸用途:
※ 在染料制造中;
※ 磺胺类药物在药物制造中占有突出地位;
※ 在制造糖精;
※ 在洗涤剂的制造中。



 购物车
购物车 



