化学反应(概念,方程式,类型)
Release Time:2021-02-09什么是化学反应?
化学反应是其中的键在反应物分子内断裂,并在产物分子内形成新键以形成新物质。化学反应无处不在,从体内食物的代谢到太阳光的吸收都是化学反应的结果。 在开始化学反应之前,了解物理和化学变化非常重要。
化学反应是其中的键在反应物分子内断裂,并在产物分子内形成新键以形成新物质。化学反应无处不在,从体内食物的代谢到太阳光的吸收都是化学反应的结果。 在开始化学反应之前,了解物理和化学变化非常重要。

燃烧的蜡烛是物理和化学变化的最好例子。拿一支蜡烛点燃。随着时间的流逝,我们可以观察到蜡烛变成蜡。如果用罐子盖住蜡烛,蜡烛将熄灭。在演示中,蜡烛的燃烧是化学变化,而蜡烛到蜡的转化是物理变化。在物理变化中,物质的状态基本上会发生变化,但是在化学变化的情况下,大多数情况下会形成新物质,其中释放或吸收能量。因此,我们可以得出结论,化学变化伴随着某些物理变化。
化学反应的基本概念
化学反应是两个或两个以上分子相互作用形成新产物时发生的过程。相互作用生成新化合物的化合物称为反应物,而新形成的化合物称为产物。化学反应在不同的行业,习惯甚至我们的日常生活中都扮演着不可或缺的角色。它们在我们周围的环境中不断发生;例如,铁锈,陶器,葡萄酒发酵等。在化学反应中,必须发生化学变化,通常会观察到物理变化,例如沉淀,发热,颜色变化等。反应可以在两个原子或离子或分子之间发生,它们形成新的键,没有原子被破坏或产生,但由反应物形成新产物。反应速率取决于压力,温度,反应物浓度等因素并受其影响。
化学反应方程式:
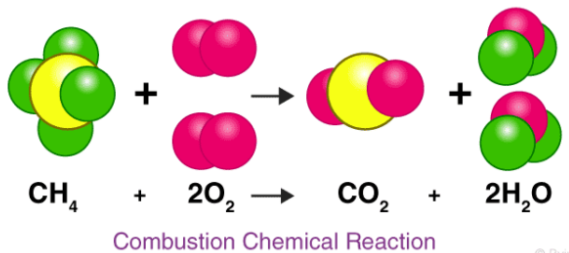
由于我们周围发生大量化学反应,因此开发了一种命名法,以简化我们如何以化学方程式形式表达化学反应。 化学方程式不过是数学表达式,它表示从反应物形成的产物,同时说明了如何进行反应的某些条件。反应物在左侧,而在右侧形成的产物通过单头或双头箭头连接。 例如反应
化学反应类型
不同类型反应的基础是形成的产物,发生的变化,涉及的反应物等。反应类型有:燃烧反应,分解反应,中和反应,氧化还原反应,沉淀或双位移反应,合成反应
1.燃烧反应
燃烧反应是指可燃物与氧化剂的反应,生成氧化产物。 氧化剂是燃料燃烧所需的化学物质,通常是氧气。 考虑一下镁金属燃烧的例子。
2Mg + O2→2MgO +热
在此,两个镁原子与一个氧分子发生反应,从而生成两个分子的氧化镁化合物,从而在此过程中释放出一些热量。
2.分解反应
分解反应是指一种成分分解成多种产物的反应。 必须改变环境中的某些能量,例如化合物的热,光或电断开键。 考虑一下碳酸钙分解产生的CaO(生石灰)的例子,CaO是水泥的主要成分。
CaCO3→热CaO + CO2(g)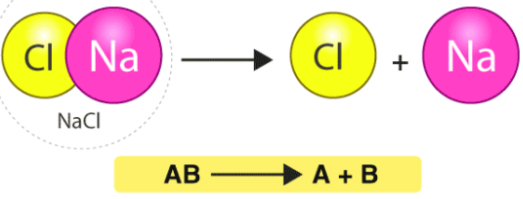
3.中和反应
中和反应基本上是酸和碱之间的反应,产生盐和水作为产物。形成的水分子是由OH-离子和H +离子组合而成。当强酸和强碱进行中和反应时,产品的总pH为7。以盐酸与氢氧化钠中和生成氯化钠(普通盐)和水的中和反应为例。
HCl + NaOH→NaCl + H2O
在此,酸和碱,盐酸和氢氧化钠在中和反应中反应,生成氯化钠(普通盐)和水作为产物。
4.氧化还原反应
REDuction-氧化反应是一种化学物种之间存在电子转移的反应。让我们以锌和氢之间的电化学电池样氧化还原反应为例。
Zn + 2H +→Zn2 ++ H2
在此,锌原子与2个带正电的氢离子发生反应,电子从锌原子转移到该离子上,并且氢成为稳定的分子,并且锌离子就是产物。
5.沉淀或双位移反应
这是一种置换反应,其中两种化合物发生反应,因此它们的阴离子和阳离子交换位置,从而形成两种新产物。考虑一下硝酸银和氯化钠之间反应的例子。经过两次置换反应后的产物将为氯化银和硝酸钠。
AgNO3 + NaCl→AgCl + NaNO3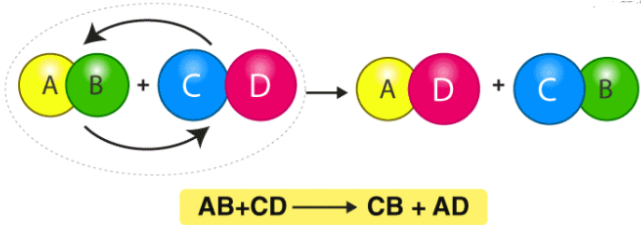
6.合成反应
合成反应是最基本的反应类型之一,其中多种简单化合物在一定的物理条件下结合,生成复杂的产物。 该产品将始终是化合物。 让我们考虑氯化钠与反应物固体钠和氯化物气体的合成反应。
2Na + Cl(g)→2NaCl
在这里,我们有2个固态钠原子与氯气反应,生成氯化钠。 食盐为产品。
化学反应的基本概念
化学反应是两个或两个以上分子相互作用形成新产物时发生的过程。相互作用生成新化合物的化合物称为反应物,而新形成的化合物称为产物。化学反应在不同的行业,习惯甚至我们的日常生活中都扮演着不可或缺的角色。它们在我们周围的环境中不断发生;例如,铁锈,陶器,葡萄酒发酵等。在化学反应中,必须发生化学变化,通常会观察到物理变化,例如沉淀,发热,颜色变化等。反应可以在两个原子或离子或分子之间发生,它们形成新的键,没有原子被破坏或产生,但由反应物形成新产物。反应速率取决于压力,温度,反应物浓度等因素并受其影响。
化学反应方程式:
由于我们周围发生大量化学反应,因此开发了一种命名法,以简化我们如何以化学方程式形式表达化学反应。 化学方程式不过是数学表达式,它表示从反应物形成的产物,同时说明了如何进行反应的某些条件。反应物在左侧,而在右侧形成的产物通过单头或双头箭头连接。 例如反应
A + B→C + D
在此,A和B是反应物,它们反应形成产物C和D。在实际的化学方程式中,反应物由其化学式表示。 为了确保质量守恒定律,必须平衡化学方程式,即两侧的原子数必须相等。 这是方程式的平衡。让我们考虑甲烷(CH 3)和氧气(O 2)之间的实际化学反应。

在这里,我们可以看到质量守恒定律表明,左侧每个原子的数量如何在右侧达到平衡。
化学反应类型
不同类型反应的基础是形成的产物,发生的变化,涉及的反应物等。反应类型有:燃烧反应,分解反应,中和反应,氧化还原反应,沉淀或双位移反应,合成反应
1.燃烧反应
燃烧反应是指可燃物与氧化剂的反应,生成氧化产物。 氧化剂是燃料燃烧所需的化学物质,通常是氧气。 考虑一下镁金属燃烧的例子。
2Mg + O2→2MgO +热
在此,两个镁原子与一个氧分子发生反应,从而生成两个分子的氧化镁化合物,从而在此过程中释放出一些热量。
2.分解反应
分解反应是指一种成分分解成多种产物的反应。 必须改变环境中的某些能量,例如化合物的热,光或电断开键。 考虑一下碳酸钙分解产生的CaO(生石灰)的例子,CaO是水泥的主要成分。
CaCO3→热CaO + CO2(g)

3.中和反应
中和反应基本上是酸和碱之间的反应,产生盐和水作为产物。形成的水分子是由OH-离子和H +离子组合而成。当强酸和强碱进行中和反应时,产品的总pH为7。以盐酸与氢氧化钠中和生成氯化钠(普通盐)和水的中和反应为例。
HCl + NaOH→NaCl + H2O
在此,酸和碱,盐酸和氢氧化钠在中和反应中反应,生成氯化钠(普通盐)和水作为产物。
4.氧化还原反应
REDuction-氧化反应是一种化学物种之间存在电子转移的反应。让我们以锌和氢之间的电化学电池样氧化还原反应为例。
Zn + 2H +→Zn2 ++ H2
在此,锌原子与2个带正电的氢离子发生反应,电子从锌原子转移到该离子上,并且氢成为稳定的分子,并且锌离子就是产物。
5.沉淀或双位移反应
这是一种置换反应,其中两种化合物发生反应,因此它们的阴离子和阳离子交换位置,从而形成两种新产物。考虑一下硝酸银和氯化钠之间反应的例子。经过两次置换反应后的产物将为氯化银和硝酸钠。
AgNO3 + NaCl→AgCl + NaNO3

6.合成反应
合成反应是最基本的反应类型之一,其中多种简单化合物在一定的物理条件下结合,生成复杂的产物。 该产品将始终是化合物。 让我们考虑氯化钠与反应物固体钠和氯化物气体的合成反应。
2Na + Cl(g)→2NaCl
在这里,我们有2个固态钠原子与氯气反应,生成氯化钠。 食盐为产品。




 购物车
购物车 



